
创建自己的小题库
搜索

化学键与化学反应中能量变化的关系题库
题数
2000
考试分类
高中化学>化学键与化学反应中能量变化的关系
售价
¥30
 手机预览
手机预览
收藏
分享
去刷题
简介
高中化学-化学键与化学反应中能量变化的关系
...更多



0道

0道

0道



章节目录
题目预览(可预览10题)
【简答题】

[1/2000]下列现象与氢键有关的是: ①水结成冰体积膨胀,密度变小 ②水加热到很高温度都难以分解 ③HF、HCl、HBr、HI的热稳定性依次减弱 ④对羟基苯甲醛的...
参考答案:
|
A
|
参考解析:
①水结成冰时分子排列为有序,使体积膨胀,密度变小,与氢键有关。正确。②水加热到很高温度都难以分解,说明水分子内的化学键结合力强,难断裂,与氢键强弱无关。错误。③HF、HCl、HBr、HI的热稳定性依次减弱与分子内的化学键强弱有关,而与物质的分子间作用力无关,也与氢键无关。错误。④对羟基苯甲醛的沸点高于邻羟基苯甲醛是由于在对羟基苯甲醛的分子之间存在氢键,增加了分子之间的相互吸引力。正确。⑤Cl 2、Br 2、I 2单质都是由分子构成的物质。结构相似。分子的相对分子质量越大,分子之间的作用力就越大,克服分子之间的作用力使物质熔化或汽化消耗的能量就越高,即熔点随相对分子质量增大而升高。但是与氢键无关。错误。⑥NH 3极易溶于水中,由于在氨分子与水分子之间容易形成氢键。正确。与氢键有关现象的是①④⑥。选项为A。
【简答题】

[2/2000]下列物质的水溶液能发生离子反应的是( ) A.Ba(NO 【图片】) 【图片】溶液与NaOH溶液B.Na 【图片】CO 【图片】溶液与稀硫酸...
参考答案:
|
B
|
参考解析:
若通过离子交换能产生沉淀、气体或难电离物质,则能发生离子反应。综合比较,只有B选项中Na
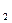 CO
CO
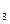 电离出来的CO
电离出来的CO
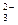 与稀H
与稀H
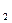 SO
SO
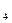 电离出来的H+反应可生成CO
电离出来的H+反应可生成CO
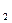 气体和H
气体和H
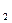 O,符合复分解反应发生的条件。
O,符合复分解反应发生的条件。
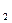 CO
CO
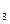 电离出来的CO
电离出来的CO
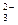 与稀H
与稀H
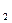 SO
SO
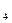 电离出来的H+反应可生成CO
电离出来的H+反应可生成CO
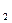 气体和H
气体和H
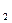 O,符合复分解反应发生的条件。
O,符合复分解反应发生的条件。
【简答题】

[3/2000]下列六种物质的变化中,将合适序号填写在下列空白中:①干冰的升华; ②硫酸钾熔化; ...
参考答案:
| ①干冰属于分子晶体,融化时克服分子间作用力; ②硫酸钾属于离子晶体,融化时破坏离子键; ③氯化钠属于离子晶体,溶于水破坏离子键; ④HCl属于分子晶体,但溶于水时发生电离,破坏共价键; ⑤氨气属于分子晶体,受热蒸发是克服的是分子间作用力; ⑥为离子晶体,含有离子键和共价键,与水反应发生化学变化,离子键和共价键都发生变化. 故答案为:(1)①⑤;(2)⑥;(3)④;(4)②③. |
参考解析:
无
【简答题】

[4/2000]以下能级符号不正确的是( ) A.2dB.3sC.4pD.5f
参考答案:
|
A
|
参考解析:
无
【简答题】

[5/2000]拆开1 mol H-H键、1 mol N-H键以及1mol N≡N键分别需要吸收的能量...
参考答案:
| (1)放出;92 kJ (2)放出;30.67 kJ |
参考解析:
无
【简答题】

[6/2000]下列物质中既含有离子键又含有共价键的是( ) A.NaOHB.NaClC.H2OD.NH4Cl
参考答案:
| A、钠离子和氢氧根之间是离子键,氢氧根内部存在共价键,故A正确; B、氯化钠中只存在钠离子和氯离子之间的离子键,故B错误; C、水分子中只有共价键,故C错误; D、所有的铵盐中既有离子键又有共价键,故D正确. 故选AD. |
参考解析:
无
【简答题】

[7/2000]下列说法正确的是 ( ) A.钠与氯气反应生成氯化钠后,其结构的稳定性增强B.阴阳离子之间...
参考答案:
|
A
|
参考解析:
阴阳离子之间有强烈的吸引作用又有排斥作用,失电子难的原子获得电子的能力不一定强比如稀有气体。两个相邻原子之间的强烈相互作用叫化学键。
【简答题】

[8/2000]下列说法正确的是( ) A.键能越大,表示该分子越容易受热分解B.共价键都具有方向性C.在分子中,两个成键的原子间...
参考答案:
|
D
|
参考解析:
无
【简答题】

[9/2000]下列物质溶于水中,既破坏离子键又破坏共价键的是 A.HClB.NaHSO4C.C2H5OHD.NaOH
参考答案:
|
B
|
参考解析:
一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键,据此可知氯化氢中含有共价键,溶于水破坏的是共价键。硫酸氢钠中含有离子键和共价键,溶于水电离出离子,既破坏离子键又破坏共价键。乙醇中含有共价键,但属于非电解质,溶于水化学键不变。氢氧化钠含有共价键和离子键,溶于水电离出钠离子和OH -,破坏的是离子键,共价键不变,答案选B。
点评:该题是高考中的常见考点,属于基础性试题的考查。该题的关键是明确离子键和共价键的含义、判断依据,以及化合物溶于水的电离情况。
【简答题】

[10/2000]已知:25℃、101kPa时,(1)12g石墨不完全燃烧生成CO,放出110.5kJ热量,CO继续燃烧又放出283.0kJ热量;(2)金刚石燃烧的热化...
参考答案:
|
D
|
参考解析:
略

 复制链接
复制链接 新浪微博
新浪微博 分享QQ
分享QQ 微信扫一扫
微信扫一扫





