
创建自己的小题库
搜索

离子共存题库
题数
2000
考试分类
高中化学>离子共存
售价
¥30
 手机预览
手机预览
收藏
分享
去刷题
简介
高中化学-离子共存
...更多



0道

0道

0道



章节目录
题目预览(可预览10题)
【简答题】

[1/2000]关于溶液的下列说法正确的是( ) A.c(H+):c(OH-)=1:10-2的溶液中K+、Ba2+、ClO-、CO32-一定能...
参考答案:
|
D
|
参考解析:
A、c(H +):c(OH -)=1:10 -2的溶液显酸性,故与CO 3 2 -不能共存;B、由水电离产生的H +浓度为1×10 -13mol•L -1的溶液,溶液为酸或碱溶液,酸性溶液中H +、NO 3-、I -发生氧化还原反应,则不能共存;C、温度不变,电离常数不变;D.等物质的量浓度的下列溶液:①H 2CO 3②Na 2CO 3③NaHCO 3④(NH 4) 2CO 3中c(CO 3 2 -)的大小关系为:②>④>③>①。
【简答题】

[2/2000]已知0.02 mol·L -1CH 3COOH溶液和0.01 mol·L -1NaOH溶液以等体积混和后溶液呈酸性,则该混合液中微粒浓度关系正确的 (...
参考答案:
|
A
|
参考解析:
已知0.02 mol·L -1CH 3COOH溶液和0.01 mol·L -1NaOH溶液以等体积混和后溶液呈酸性,相当于是醋酸和醋酸钠等体积等浓度混合,显示酸性,说明醋酸的电离程度大于醋酸根的水解程度;所以 c (CH 3COO -)> c (Na +) ; c (CH 3COOH)> c (CH 3COO -) ;由电荷守恒: c (Na +) + c (H +) = c (OH -) + c (CH 3COO -)所以 c (Na +) + c (H +) < c (OH -) + c (CH 3COOH)+ c (CH 3COO -) ; c (CH 3COOH)+ c (CH 3COO -)="0.01" mol·L -1 ,故选A。
点评:醋酸的电离程度大于醋酸根的水解程度,所以醋酸和醋酸钠等体积等浓度混合后,显酸性,在计算时,可以这样考虑,如果正好显示中性,则, c (CH 3COO -)= c (Na +) ,但是醋酸的电离程度大于醋酸根的水解程度,所以 c (CH 3COO -)> c (Na +)。
【简答题】

[3/2000]下列离子在溶液中能大量共存的是( )。 A.Na+、CO32-、SO42-、H+B.K+、AlO2-、H+、Cl-C...
参考答案:
|
D
|
参考解析:
离子间如果发生化学反应,则不能大量共存,反之可以。A中生成CO
2和水,B中生成氢氧化铝沉淀,C中在酸性条件下NO
3
-能和Fe
2
+,所以正确的答案选D。
【简答题】

[4/2000]常温下,下列各组离子在指定溶液中能大量共存的是( ) A.pH=1的溶液中:Fe 【图片】、NO 【图片】、SO 【图片】、Na 【图片】B.由水电...
参考答案:
|
C
|
参考解析:
离子间如果发生化学反应,就不能大量共存,反之可以。A中溶于显酸性,Fe
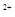 和NO
和NO
 发生氧化还原反应。B中溶液中水的电离被抑制,因此溶于可能显酸性,也可能显碱性。HCO
发生氧化还原反应。B中溶液中水的电离被抑制,因此溶于可能显酸性,也可能显碱性。HCO
 和氢离子或OH
-都反应,不能大量共存。根据水的离子积常数可知,选项C中溶液显酸性,可以大量共存。D中铁离子和SCN
-会发生化学反应,不能大量共存。答案选C。
和氢离子或OH
-都反应,不能大量共存。根据水的离子积常数可知,选项C中溶液显酸性,可以大量共存。D中铁离子和SCN
-会发生化学反应,不能大量共存。答案选C。
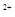 和NO
和NO
 发生氧化还原反应。B中溶液中水的电离被抑制,因此溶于可能显酸性,也可能显碱性。HCO
发生氧化还原反应。B中溶液中水的电离被抑制,因此溶于可能显酸性,也可能显碱性。HCO
 和氢离子或OH
-都反应,不能大量共存。根据水的离子积常数可知,选项C中溶液显酸性,可以大量共存。D中铁离子和SCN
-会发生化学反应,不能大量共存。答案选C。
和氢离子或OH
-都反应,不能大量共存。根据水的离子积常数可知,选项C中溶液显酸性,可以大量共存。D中铁离子和SCN
-会发生化学反应,不能大量共存。答案选C。
【简答题】

[5/2000]无论是加酸还是加碱能使离子数目减少的是 &n...
参考答案:
|
C
|
参考解析:
略
【简答题】

[6/2000]在某无色透明的酸性溶液中,能共存的离子组是 [ ] A. 【图片】 B. 【图片】 C. 【图片】 D...
参考答案:
| C |
参考解析:
无
【简答题】

[7/2000]某溶液中含有Na +、CO 32-、 HCO 3-、 SO 32-、 Cl -,在加入Na 2O 2后浓度不发生变化的是 A.Na+、CO32- B....
参考答案:
|
B
|
参考解析:
Na 2O 2具有强氧化性,与水反应后溶液呈碱性,具有还原性的离子和能与OH -反应的离子浓度发生改变。A、Na 2O 2与水反应后生成NaOH,使Na +离子浓度增大,HCO 3 -与OH -反应,HCO 3 -离子浓度减小,生成故CO 3 2 -,CO 3 2 -离子浓度增大,故A错误; B、Cl -离子浓度基本不变,故B正确;C、Na 2O 2与水反应后生成NaOH,使Na +离子浓度增大,HCO 3 -与OH -反应,HCO 3 -离子浓度减小,生成故CO 3 2 -,CO 3 2 -离子浓度增大;Cl -离子浓度基本不变,故C错误;D、Na 2O 2具有强氧化性,将SO 3 2-氧化为SO 4 2-,则SO 3 2-离子浓度减小,Na 2O 2与水反应后生成NaOH,HCO 3 -与OH -反应,HCO 3 -离子浓度减小,故D错误
【简答题】

[8/2000]活性氧化锌用作橡胶硫化的活性剂、补强剂。以氧化锌粗品为原料制备活性氧化锌的生产工艺流程如下: 【图片】一些阳离子以氢氧化物形式完全沉淀时溶液的pH见下...
参考答案:
|
(1)增大固液接触面积,加快溶解时的反应速率(4分)
(2)Na 2CO 3(2分) 0.003 (3分) (3)锌粉(3分) (4) 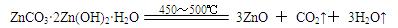 (4分) (4分)
|
参考解析:
略
【简答题】

[9/2000]下列各组离子能大量共存于同一水溶液中的是( ) A.HCO3-、Na+、K+、H+B.NO3-、Cl-、Na+、Ag+C.Mg2+、K+、NO3-、...
参考答案:
| A、因HCO3-、H+能结合生成水和二氧化碳气体,则不能大量共存,故A错误; B、因Cl-、Ag+能结合生成AgCl沉淀,则不能大量共存,故B错误; C、因Mg2+、OH-能结合生成氢氧化镁沉淀,则不能大量共存,故C错误; D、因该组离子之间不反应,则能大量共存,故D正确; 故选D. |
参考解析:
无
【简答题】

[10/2000]某强酸性溶液X中可能含有Na +、K +、NH 4+、Fe 2+、A1 3+、CO 32―、SO 32―、SO 42―、C1 ―、NO 2-中的若干种...
参考答案:
|
D
|
参考解析:
①强酸性溶液中CO 3 2―、SO 3 2―、NO 2 - 不能存在;② X溶液中加入过量Ba(NO 3) 2溶液生成沉淀C是BaSO 4,说明有SO 4 2―存在;生成气体A为NO,说明有Fe 2+存在,(即3 Fe 2++4H ++ NO 3 - =" 3" Fe 3++NO↑+2H 2O)。③ 溶液B加入过量NaOH溶液,生成的沉淀G为Fe(OH) 3;生成的气体F为NH 3,说明有NH 4 +存在。④ 溶液H通入CO 2生成沉淀I,由于前面加入过量的Ba(NO 3) 2溶液,引入了大量Ba 2+,所以沉淀I中一定有BaCO 3,又由于前面不能确定溶液X中是否存在A1 3+,所以这里也不能确定沉淀I中有A1(OH) 3;溶液J的焰色反应呈黄色,说明溶液J中有Na +,但由于前面加入过量NaOH溶液,引入了较多的Na +,因此不能确定溶液X中是否存在Na +;因为焰色黄色能掩盖紫色焰色,所以不能确定溶液X中是否有K +;另外,上述实验过程还不能确定溶液X中是否存在C1 ―。

 复制链接
复制链接 新浪微博
新浪微博 分享QQ
分享QQ 微信扫一扫
微信扫一扫





