
创建自己的小题库
搜索

查理定律(等容定律)题库
题数
113
考试分类
高中物理>查理定律(等容定律)
售价
¥15
 手机预览
手机预览
收藏
分享
去刷题
简介
高中物理-查理定律(等容定律)
...更多



0道

0道

0道



章节目录
题目预览(可预览10题)
【简答题】

[1/113]请回答下列有关DIS实验“研究气体的压强与体积的关系”的问题.(1)如图所示,用一个带有刻度的注射器及DIS实验系统来探究气体的压强与体积关系.实验中...
参考答案:
| (1)用DIS实验“研究气体的压强与体积的关系”时,气压用压强传感器测量; (2)A、B、玻意耳定律成立的前提是等温且质量一定,故A正确,B正确; C、玻意耳定律成立的前提是等温且质量一定,气体质量具体值不需要测量,故C错误; D、玻意耳定律成立的前提是等温且质量一定,单位可以不用国际单位,故D错误; (3)A、实验时注射器活塞与筒壁间的摩擦力不断增大,不会影响气压与体积,故A错误; B、实验时环境温度增大了,根据理想气体状态方程
C、封闭气体压强与外界大气压强无关,故C错误; D、实验时注射器的空气向外发生了泄漏,根据理想气体状态方程
故选D. 故答案为:(1)压强;(2)AB;(3)D. |
参考解析:
PVT
【简答题】

[2/113]一个“┌”型细玻璃管A、B两端开口,水平段内有一段长为5cm的水银柱,初始时长度数据如图所示.现将玻璃管B端封闭,然后将下端A插入大水银槽中,整个过程...
参考答案:
| (1)竖直段部分封闭气体初始状态:P1=75cmHg,L1=70cm 稳定后:P2=75+5=80cmHg, 等温变化,则P1L1S=P2L2S 得L2=62.625cm>60cm,所以水银柱还是在水平段管内. 稳定后B端水平段内气体压强P′2=P2=80cmHg. (2)稳定后水平段内气体长度L′2=
进入竖直管内的水银长度为△h=60+35-18.75-5-62.625=8.625cm 竖直管插入水银槽的深度h=8.625+5=13.625cm. 答:(1)稳定后玻璃管B端水平段内被封闭气体的压强为80cmHg; (2)竖直管A端插入水银槽的深度h为13.625cm. |
参考解析:
P′1
L′1
P′2
【简答题】

[3/113]开尔文运用合理外推的方法,建立起热力学温标,所利用的实验事实是一定质量的气体( ) A.压强不变,体积与摄氏温度成正比 B.体...
参考答案:
| D |
参考解析:
无
【简答题】

[4/113]一定量的理想气体与两种实际气体I、II在标准大气压下做等压变化时的V-T关系如图(a)所示,图中V-V0V0-V″ =12.用三份上述理想气...
参考答案:
| 可以从(a)图看出,实际气体Ⅰ由温度T1升高到温度T0时,体积膨胀的多,实际气体Ⅱ由温度T1升高到温度T0时,体积膨胀的少.当制成温度计时,在T1温度时,三种气体温度相同,当温度升高到T0时,Ⅱ气体体积膨胀的少,气体体积小,温度计示数低.所以Ⅱ温度计中的物质是气体Ⅱ. 在温度为T0时,Tⅱ=21℃,Tⅲ=24℃,由于
Ⅰ气体使实际值偏大,Ⅱ气体使实际值偏小,根据数据关系,体积比应该是2:1. 故答案为:II; 23; 2:1 |
参考解析:
无
【简答题】

[5/113]一根两端开口、横截面积为S=2cm2足够长的玻璃管竖直插入水银槽中并固定(插入水银槽中的部分足够深).管中有一个质量不计的光滑活塞,活塞下封闭着长L=...
参考答案:
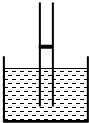 (1)被封闭气体的初状态为 P1=P0=1.0×105Pa=75cmHg, V1=LS=21S,T1=280K 末态为P2=P0=1.0×105Pa=75cmHg, V2=L2S,T2=320K 根据盖?吕萨克定律,
故此时气柱为24cm. (2)在活塞上施加拉力F后,根据活塞受力平衡得: F+P3S=P0S P3=0.8×105Pa 气体的状态变为 V3=L3S,T3=T2=320K 根据玻意耳定律, P2V2=P3V3 得:L3=30cm 而 P3=0.8×105Pa (相当于60cm汞柱高的压强)所以管内外水银面的高度差为 △h=15cm. 故平衡后气柱为30cm,管内外水银面的高度差为15cm. |
参考解析:
无
【简答题】

[6/113]如图所示是一定质量的气体从状态A经过状态B 到状态C的p-T图象,由图象可知 【图片】 [ ] A.V...
参考答案:
| AC |
参考解析:
无
【简答题】

[7/113]如图所示,四支两端封闭、粗细均匀的玻璃管内的空气被一段水银柱隔开,按图中标明的条件,当玻璃管水平放置时,水银柱处于静止状态。如果管内两端的空气都升高相...
参考答案:
| CD |
参考解析:
无
【简答题】

[8/113]某压力锅结构如图所示。盖好密封锅盖,将压力阀套在出气孔上,给压力锅加热,当锅内气体压强达到一定值时,气体就把压力阀顶起。假定在压力阀被顶起时,停止加热...
参考答案:
解:(1)设锅内气体分子数为n  (2)根据热力学第一定律得:ΔU=W+Q=-3 J 锅内气体内能减少,减少了3 J (3)由P=P0(1-αH)(其中α>0)知,随着海拔高度的增加,大气压强减小 由  知,随着海拔高度的增加,阀门被顶起时锅内气体压强减小 知,随着海拔高度的增加,阀门被顶起时锅内气体压强减小根据查理定律得:  可知阀门被顶起时锅内气体温度随着海拔高度的增加而降低 |
参考解析:
无
【简答题】

[9/113]如图所示,内截面积为S=10-4m2、足够高的圆柱形气缸开口向上竖直放置在水平面上,缸内离底部高为h1=0.08m处有一质量为m=0.2kg的活塞封住...
参考答案:
解;(1)初态:P1=P0+
封闭气体做等容变化,根据查理定律得:
代入数据求得:p2=1.5×105Pa (2)P3=P0-
封闭气体做等温变化,根据玻意耳定律得:p1h1S=p3h2S 代入数据求得:h2=12cm 答:(1)缸内气体的压强p2为1.5×105Pa (2)活塞与气缸底的距离h2为12cm. |
参考解析:
mgs
【简答题】

[10/113]甲、乙两个相同的密闭容器中分别装有等质量的同种气体,已知甲、乙容器中气体的压强分别为p甲、p乙,且p甲<p乙,则 [ ...
参考答案:
| BC |
参考解析:
无

 复制链接
复制链接 新浪微博
新浪微博 分享QQ
分享QQ 微信扫一扫
微信扫一扫





