
创建自己的小题库
搜索

有机化学的有关计算题库
题数
772
考试分类
高中化学>有机化学的有关计算
售价
¥25
 手机预览
手机预览
收藏
分享
去刷题
简介
高中化学-有机化学的有关计算
...更多



0道

0道

0道



章节目录
题目预览(可预览10题)
【简答题】

[1/772]近年合成了一种新化合物,本题用X为代号。用现代物理方法测得X的相对分子质量为64;X含碳93.8%,含氢6.2%;X分子 中有3种化学环境不同的氢原子...
参考答案:
| (1)C5H4 (2)  |
参考解析:
无
【简答题】

[2/772]现有0.2mol有机物于0.5mol氧气在一密闭容器中燃烧,得产物为CO2、CO、H2O.产物通过浓硫酸时,浓硫酸的质量增加10.8g;通过灼热氧化铜...
参考答案:
(1)浓硫酸增重10.8g说明反应产物中含水10.8g,即产物中含水
通过灼热氧化铜,氧化铜质量减轻3.2g, CO+CuO
1mol 1mol 16g 0.2mol 0.2mol
说明CO还原氧化铜反应中氧化铜失去O为3.2g,即0.2mol, 同时说明产物中含0.2molCO, 通过碱石灰增重17.6g说明还原氧化铜的得到的CO2与原产物的CO2总重17.6g,即0.4mol,减去由CO转化来的0.2moCO2l,说明产物中含 0.2molCO2. 通过上述分析,可以知道0.2mol有机物与 0.5mol氧气 反应生成0.6molH2O、0.2molCO、0.2molCO2, 即 1.2molH,1.2molO,0.4molC,减去参与反应的0.5molO2,即1molO, 可得知0.2mol 的有机物含有1.2molH,0.2molO,4molC0, 即:1mol有机物含 6molH,1molO,2molC,化学式为C2H6O, 答:有机物的分子式为C2H6O. (2)分子式为C2H6O的有机物可能为乙醇结构式CH3-CH2-OH,甲醚结构式CH3-O-CH3 均符合. 答:该有机物可能的结构简式为CH3-CH2-OH或CH3-O-CH3. |
参考解析:
10.8g18g/mol
【简答题】

[3/772](9分)根据要 【图片】求填空: (1)写出下列有机物的键线式: 【图片】 _____ ▲ ______ CH 3CH...
参考答案:
|
(9分)(1)
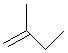 ; ;
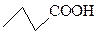
(2)2,3,5-三甲基-4-乙基庚烷 (3)略 (4)2种 (5)CH 2="CHCN; " CH 2=CH-CH=CH 2; CH 2=CH 2; (每空1分) |
参考解析:
略
【简答题】

[4/772]下列关于有机物的说法正确的是 A.乙醇、乙烷和乙酸都可以与钠反应生成氢气B.淀粉、脂肪和蛋白质在一定条件下都能发生水解反应C.苯和乙烯都可使溴的四氯化...
参考答案:
|
B
|
参考解析:
无
【简答题】

[5/772]石油化工是江苏省的支柱产业之一。聚氯乙烯是用途十分广泛的石油化工产品,某化工厂曾利用下列工艺生产聚氯乙烯的单体氯乙烯:CH2=CH2+Cl2→CH2C...
参考答案:
| (1)5.8;3.4 (2)设投入反应①、③的乙烯物质的量分别为x、y,则: 由反应①生成的二氯乙烷为x·a%, 由反应③生成的二氯乙烷为y·c%, 则由反应①、③共制得二氯乙烷的物质的量为(x·a%+y·c%),通过反应②可获得HCl的物质的量为 (x·a%+y·c%)·b%。据题意,反应③消耗的HCl为2·y·c%,则:2·y·c%=(x·a%+y·c%)·b% |
解得: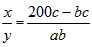 反应①、③中乙烯的投料比应为 反应①、③中乙烯的投料比应为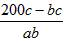 。 。 |
参考解析:
无
【简答题】

[6/772](三选一)【化学一选修5:有机化学基础】由碳、氢、氧三种元素组成的有机物A,其相对分子质量为118,A中含氢的质量分数为8.5%,分子中氢原子个数为碳...
参考答案:
(1) (2)①  ;②cd ;②cd(3)   (任意一个即可) (任意一个即可)(4)  (5)  |
参考解析:
无
【简答题】

[7/772]A是含C、H、O三种元素的有机物,如果已知下列相关物理量,则可以确定A的分子式:(1)碳的质量分数 【图片】(2)氢的质量分数 【图片】(3)A的质量...
参考答案:
| B |
参考解析:
无
【简答题】

[8/772]鲨鱼不患癌症,是因为其体内含有的角鲨烯具有抗癌性,实验测得角鲨烯分子是链状结构,分子中含有30 个碳原子且碳、氢质量比为7.2:1,下列说法中不正确的...
参考答案:
| B |
参考解析:
无
【简答题】

[9/772](1)合成材料 【图片】被涂在手术伤口表面,在数秒内发生固化(加聚)并粘结以代替通常的缝合,是一种性能优良的功能高分子材料。写出该化合物固化时的化学反...
参考答案:
(1) (2)1.01×104 ;  +3nO2→2nCO2+2nH2O ;67.2L +3nO2→2nCO2+2nH2O ;67.2L |
参考解析:
无
【简答题】

[10/772]某链烃A1mol,在一定条件下完全分解(裂解)成1mol烷烃B和1mol烯烃C,生成的混合气体对氢气的相对密度为14.5.通过计算回答下列问题:(1)...
参考答案:
| (1)CH3CH2CH2CH3 正丁烷 CH3C(CH3)CH3 异丁烷 (2)B为甲烷,C为丙烯或B为乙烷,C为乙烯 (3)C只能是丙烯 |
参考解析:
无

 复制链接
复制链接 新浪微博
新浪微博 分享QQ
分享QQ 微信扫一扫
微信扫一扫





