
创建自己的小题库
搜索

极性分子、非极性分子题库
题数
710
考试分类
高中化学>极性分子、非极性分子
售价
¥25
 手机预览
手机预览
收藏
分享
去刷题
简介
高中化学-极性分子、非极性分子
...更多



0道

0道

0道



章节目录
题目预览(可预览10题)
【简答题】

[1/710]据新浪科技网报道:美国科学家发现,普通盐水在无线电波的照射下可以燃烧,这很可 能是21世纪人类最伟大的发现之一,将有望解决未来人类的能源危机。无线电频...
参考答案:
|
B
|
参考解析:
无
【简答题】

[2/710](14分)X、Y、Z三种元素,原子序数依次减小。X是第四周期主族元素,其部分电离能如图17所示;X、Y元素具有相同的最高正化合价;Z元素是形成化合物种...
参考答案:
|
(14分,每空2分)(1)Mg
3N
2 (2分) 离子晶体
(2分)
(2)< (2分)(3)B、D (2分) (4)12 (2分)(5)低(2分)CaO、MgO都是离子晶体,Ca 2 +半径比Mg 2 +大,CaO晶格能小,熔点低 (2分) |
参考解析:
根据X的电离能可知,X的最高价是+2价,所以X是钙,则Y是镁。Z元素是形成化合物种类最多的元素,所以Z是碳元素。
(1)镁的最高价是+2价,氮元素的最低价是-3价,二者都是活泼的金属和非金属,所以形成的化学键是离子键,化合物是离子化合物,化学式为Mg 3N 2。
(2)金属性越强,电负性越小,所以X的电负性小于Y的。
(3)化学式为Z 2H 4的应是乙烯,碳元素不能形成氢键,A不正确,B正确,C不正确,分子中含有碳碳双键,所以应该是5个σ键和1个π键,D正确,答案选BD。
(4)钛离子在顶点处,而氧离子在面心处,所以钛离子和周围3×8÷2=12铬氧离子相紧邻。
(5)CaO、MgO都是离子晶体,Ca 2 +半径比Mg 2 +大,CaO晶格能小,熔点低。
(1)镁的最高价是+2价,氮元素的最低价是-3价,二者都是活泼的金属和非金属,所以形成的化学键是离子键,化合物是离子化合物,化学式为Mg 3N 2。
(2)金属性越强,电负性越小,所以X的电负性小于Y的。
(3)化学式为Z 2H 4的应是乙烯,碳元素不能形成氢键,A不正确,B正确,C不正确,分子中含有碳碳双键,所以应该是5个σ键和1个π键,D正确,答案选BD。
(4)钛离子在顶点处,而氧离子在面心处,所以钛离子和周围3×8÷2=12铬氧离子相紧邻。
(5)CaO、MgO都是离子晶体,Ca 2 +半径比Mg 2 +大,CaO晶格能小,熔点低。
【简答题】

[3/710]( 13分)西瓜膨大剂别名氯吡苯脲,是经过国家批准的植物生长调节剂,实践证明长期使用对人体无害。已知其相关性质如下表所示: 分...
参考答案:
|
(13分)(1)1 (1分) (2)分子晶体 N> O> C (各1分,共2分)
(3)sp 2、sp 3 (各1分,共2分) (4)C、D (各1分,共2分) (5)氯吡苯脲是分子晶体,故熔点低;氯吡苯脲与水分子间形成氢键,故易溶于水。(各1分,共2分) (6)N A(或6.02×10 23) N A(或6.02×10 23)(各1分,共2分) |
参考解析:
无
【简答题】

[4/710]下列叙述正确的是 [ ] A.NH3是极性分子,分子中N原子是在3个H原子所组成的三角形的中心 B.C...
参考答案:
| C |
参考解析:
无
【简答题】

[5/710]现代无机化学对硫氮化合物的研究是最为活跃的领域之一。如图是已经合成的最著名的硫氮化合物的分子结构。 【图片】下列说法正确的是( ) A.该物质的...
参考答案:
|
B
|
参考解析:
它的分子式应为S
4N
4;有1 mol的该物质的微粒中含有共价键为10
N
A;同位素是针对原子而言的。
【简答题】

[6/710]电子数相等的微粒叫做等电子体,下列各组微粒属于等电子体是 ①CO和CO 2 ②NO和NO 2 ③CH 4和NH 3 ④ CO和N 2&nbs...
参考答案:
|
C
|
参考解析:
六组都是共价化合物,没有电子的得失,所以微粒的电子数等于原子电子数之和,如CO的电子数为6+8=14,而CO 2的电子数为6+2×8=22.电子数相等的有④⑥三组,故选C
点评:考查微粒电子数的计算,注意区分共价化合物和离子化合物的计算
【简答题】

[7/710]下列比较中错误的是 [ ] A.沸点:CH4> GeH4> SiH4 B.溶解性:NH3&...
参考答案:
| A |
参考解析:
无
【简答题】

[8/710]R、Q为短周期中的两种元素,R元素原子的最外层电子数与次外层电子数之差的绝对值等于电子层数;Q元素的原子比R元素的原子多2个核外电子,则下列叙述中肯定...
参考答案:
|
A
|
参考解析:
略
【简答题】

[9/710]下列微粒空间构型为平面三角形的是( ) A.NF3B.HCHOC.PCl3D.H3O+
参考答案:
|
B
|
参考解析:
HCHO中的C原子采取的是sp
2杂化,三个杂化轨道呈平面三角形,2个sp
2杂化轨道分别与一个H原子形成一个C-Hσ键,另一个sp
2杂化轨道与O原子形成一个σ键,C原子中未用于杂化的p轨道与O原子的p轨道形成一个π键,空间构型为平面三角形。NF
3、PCl
3、H
3O
+中心原子均采取sp
3杂化,4个杂化轨道呈正四面体形,由于3个杂化轨道形成化学键,有1个杂化轨道被孤对电子占据,所以分子空间构型为三角锥形。
【简答题】

[10/710](6分)A、B、C、D、E为原子序数依次增大的短周期主族元素。已知A、B、C同周期,B、D同主族,且D的原子序数是B的2倍。回答下列问题: (1)DC...
参考答案:
|
(1)角形(或V形)(1分);
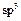 (1分) (1分)
(2)极性(1分);SO 2与水反应生成了 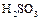 (或 (或
 或 或
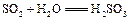 )(1分) )(1分)
(3) 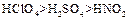 (1分); (1分);
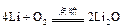 (1分) (1分)
|
参考解析:
略

 复制链接
复制链接 新浪微博
新浪微博 分享QQ
分享QQ 微信扫一扫
微信扫一扫





