
创建自己的小题库
搜索
【判断题】


采用电位滴定法,用0.20 mol.dm-3NaOH溶液滴定0.10 mol.dm-3HCl和0.10 mol.dm-3H3PO4的混合溶液时,在电位滴定曲线上,可以出现2个突跃范围。 ( )
A.
正确
B.
错误

 分享
分享
 反馈
反馈 收藏
收藏 举报
举报参考答案:

举一反三
【简答题】25℃时,用浓度为0.1000mol•L-1的NaOH溶液滴定20.00mL浓度均为0.1000mol•L-1的三种酸HX、HY、HZ滴定曲线如图所示.下列说法正确的是( )
A.
在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX
B.
根据滴定曲线,可得Ka(HY)≈10-5
C.
将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>c(OH-)>c(H+)
D.
HY与HZ混合,达到平衡时:c(H+)= Ka(HY)•c(HY) c(Y-) +c(Z-)+c(OH-)


【单选题】常温下,用0.1000mol/LHCl溶液滴定20.00mL0.1000mol/LNH3?H2O溶液滴定曲线如图.下列说法正确的是( )
A.
点①溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
B.
点②溶液中:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
C.
点③溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-)
D.
滴定过程中可能出现:c(NH3?H2O)>c(NH4+)>c(OH-)>c(Cl-)>c(H+)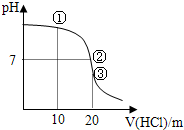

【单选题】已知25℃时,AgC1、AgBr、Agl的Ksp分别为1.8×l0 -l0 、5.O×10 —13 、8.3×10 —17 ,用AgNO 3 标准溶液滴定卤素离子的过程,以滴入AgNO 3 溶液的体积为横坐标,pX为纵坐标:[pX= -lgc(X )],就可绘得滴定曲线。现以0.1 mol·L -l AgNO 3 溶液分别滴定20.00 mL 0.1 mol·L -l Cl 、Br 、I 绘得滴定...
A.
a、b、c分别表示Cl 、Br 、I
B.
a、b、c分别表示I 、Br 、Cl
C.
a、b、c分别表示Br 、I 、Cl
D.
用硝酸银滴定法测定试样中c(Cl ),可用KI作指示剂
【单选题】常温下,用0.100 0 mol/L NaOH溶液滴定20.00 mL 0.100 0 mol/L CH 3 COOH溶液所得滴定曲线如图所示.下列说法正确的是 [ ]
A.
点①所示溶液中:c(CH 3 COO - )+c(OH - )=c(CH 3 COOH)+c(H + )
B.
点②所示溶液中:c(Na + )=c(CH 3 COOH)+c(CH 3 COO - )
C.
点③所示溶液中:c(Na + )>c(OH - )>c(CH 3 COO - )>c(H + )
D.
滴定过程中可能出现:c(CH 3 COOH)>c(CH 3 COO - )>c(H + )>c(Na + )>c(OH - )

相关题目:
【简答题】25℃时,用浓度为0.1000mol•L-1的NaOH溶液滴定20.00mL浓度均为0.1000mol•L-1的三种酸HX、HY、HZ滴定曲线如图所示.下列说法正确的是( )
A.
在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX
B.
根据滴定曲线,可得Ka(HY)≈10-5
C.
将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>c(OH-)>c(H+)
D.
HY与HZ混合,达到平衡时:c(H+)= Ka(HY)•c(HY) c(Y-) +c(Z-)+c(OH-)


【单选题】常温下,用0.1000mol/LHCl溶液滴定20.00mL0.1000mol/LNH3?H2O溶液滴定曲线如图.下列说法正确的是( )
A.
点①溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
B.
点②溶液中:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
C.
点③溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-)
D.
滴定过程中可能出现:c(NH3?H2O)>c(NH4+)>c(OH-)>c(Cl-)>c(H+)

【单选题】已知25℃时,AgC1、AgBr、Agl的Ksp分别为1.8×l0 -l0 、5.O×10 —13 、8.3×10 —17 ,用AgNO 3 标准溶液滴定卤素离子的过程,以滴入AgNO 3 溶液的体积为横坐标,pX为纵坐标:[pX= -lgc(X )],就可绘得滴定曲线。现以0.1 mol·L -l AgNO 3 溶液分别滴定20.00 mL 0.1 mol·L -l Cl 、Br 、I 绘得滴定...
A.
a、b、c分别表示Cl 、Br 、I
B.
a、b、c分别表示I 、Br 、Cl
C.
a、b、c分别表示Br 、I 、Cl
D.
用硝酸银滴定法测定试样中c(Cl ),可用KI作指示剂
【单选题】常温下,用0.100 0 mol/L NaOH溶液滴定20.00 mL 0.100 0 mol/L CH 3 COOH溶液所得滴定曲线如图所示.下列说法正确的是 [ ]
A.
点①所示溶液中:c(CH 3 COO - )+c(OH - )=c(CH 3 COOH)+c(H + )
B.
点②所示溶液中:c(Na + )=c(CH 3 COOH)+c(CH 3 COO - )
C.
点③所示溶液中:c(Na + )>c(OH - )>c(CH 3 COO - )>c(H + )
D.
滴定过程中可能出现:c(CH 3 COOH)>c(CH 3 COO - )>c(H + )>c(Na + )>c(OH - )

参考解析:


AI解析
重新生成

题目纠错 0
发布

 复制链接
复制链接 新浪微博
新浪微博 分享QQ
分享QQ 微信扫一扫
微信扫一扫





